Das Aderhautmelanom
Zuletzt aktualisiert: 14.04.2026 | Autor(in): Max Schlaak, Markus Heppt
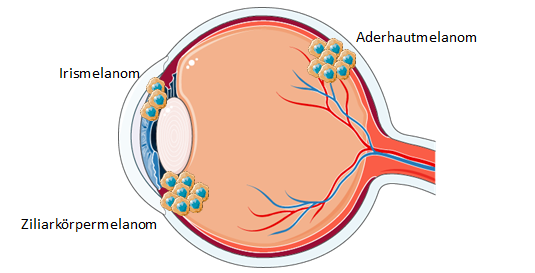
Das Aderhautmelanom stellt für Erwachsene einen der häufigsten Tumore des Auges dar. Ursächlich ist eine bösartige Vermehrung von Pigmentzellen, die zu ca. 90% im Bereich der Aderhaut und in deutlich selteneren Fällen an der Iris und dem Ziliarkörper zu finden sind (siehe Abbildung 1 (1)).
Der Tumor ist mit ca. 4-7 betroffenen Patienten/1.000.000 Einwohner insgesamt selten, es erkranken pro Jahr in Deutschland etwa 350-600 Menschen, der Altersgipfel liegt bei ca. 50-60 Jahren (2,3).
Aderhautmelanome und Melanome, die an der Haut entstehen, unterscheiden sich grundlegend in ihrer Biologie. Im Gegensatz zu malignen Melanomen der Haut finden sich in Aderhautmelanomen nur wenige Mutationen, und die Treibermutationen unterscheiden sich von denen an der Haut. Bei Aderhautmelanomen werden bis zu 80% GNAQ oder GNA11 Treibermutationen nachgewiesen (4,5).
Der Nachweis einer Monosomie 3 oder inaktivierender Mutationen in BAP-1 haben einen Einfluss auf die Prognose der Erkrankung (4,5), werden im klinischen Alltag allerdings eher selten analysiert.
Broschüre „„Aderhautmelanom – Ein Ratgeber für Patientinnen und Patienten“
Welche Symptome können auftreten?
In der frühen Phase kann ein Aderhautmelanom symptomfrei bleiben und wird dann zufällig bei einer Routineuntersuchung entdeckt. Je nach Lokalisation und Größe des Tumors können jedoch folgende Symptome auftreten:
- Sehminderung: unscharfes Sehen oder der Verlust eines Teils des Gesichtsfeldes
- Lichtblitze (Photopsien): Wahrnehmung von Lichtblitzen, insbesondere in der Dunkelheit
- Schwebende Punkte (Floater): dunkle Schatten oder „Mücken“ im Sichtfeld
- Druckgefühl oder Schmerzen: diese treten seltener auf und deuten meist auf ein
- fortgeschritteneres Stadium hin
- Veränderungen des Auges: sichtbare Pigmentierungen, deutlich erweiterte Blutgefäße auf der Lederhaut („das Weiße“ im Auge), Verformung der Pupille oder
- Farbänderung der Iris, wenn der Tumor in diese Strukturen einwächst
Die Symptome sind nicht spezifisch und können auch bei anderen Augenerkrankungen auftreten. Daher ist eine gründliche Abklärung durch einen Augenarzt/eine Augenärztin erforderlich. Wenn ein Tumorverdacht am Auge besteht, wird der Patient/die Patientin an ein spezialisiertes Zentrum zur Diagnostik oder Behandlung weitergeschickt.
Das Aderhautmelanom ist insgesamt selten, stellt aber bei Erwachsenen einen der häufigsten Augentumore dar.
Das Aderhautmelanom ist insgesamt selten, stellt aber bei Erwachsenen einen der häufigsten Augentumore dar.
Zwischen Melanomen an der Haut um im Auge bestehen große Unterschiede in der Tumorbiologie und in der Wirksamkeit von medikamentösen Therapien.
- REFERENZEN
- [1] Servier Medical Arts
- [2] Mallone S, et al. Descriptive epidemiology of malignant mucosal and uveal melanomas and adnexal skin carcinomas in Europe. Eur J Cancer. 2012
- [3] Coupland et al.: Molecular pathology of uveal melanoma. Eye (Lond). 2013
- [4] Van Raamsdonk et al.: Frequent somatic mutations of GNAQ in uveal melanoma and blue naevi. Nature. 2009
- [5] Van Raamsdonk et al.: Mutations in GNA11 in uveal melanoma. N Engl J Med. 2010
- [6] Bechrakis et al.: Das uveale Melanom – standardisiertes Vorgehen in Diagnostik, Therapie und Nachsorge. Klin Monbl Augenheilkd. 2021
- [7] Nathan et al.: Overall Survival Benefit with Tebentafusp in Metastatic Uveal Melanoma. N Engl J Med. 2021
- [8] Hassel et al.: Three-Year Overall Survival with Tebentafusp in Metastatic Uveal Melanoma. N Engl J Med. 2023
INTERESSENSKONFLIKTE
Der Autor/die Autorin hat keine Interessenskonflikte angegeben.
Diagnostik Aderhautmelanom
Zuletzt aktualisiert: 14.04.2026 | Autor(in): Max Schlaak, Markus Heppt
Es ist darauf hinzuweisen, dass bei dieser seltenen Erkrankung noch keine allgemeinen Leitlinien vorliegen.
Patientinnen und Patienten mit Aderhautmelanomen können über unspezifische Symptome wie Sehstörungen, verschwommenes Sehen, Flimmern oder Einschränkungen des Gesichtsfeldes berichten. Manchmal wird die Diagnose auch im Rahmen einer Routineuntersuchung gestellt.
Sofern der Verdacht auf ein Aderhautmelanom vorliegt, können beim Augenarzt bzw. bei der Augenärztin oder den spezialisierten Zentren folgende Untersuchungen erfolgen:
- Erhebung der Krankengeschichte des Patienten
- Sehtest
- Messung des Augeninnendrucks
- Spiegelung des Augenhintergrunds
- Fotodokumentation/ Weitwinkelbildgebung
- Echographie
- Magnetresonanztomographie (MRT)
- Ggfls. feingewebliche Untersuchungen durch Probebiopsien
- Ggfls. molekulargenetische Aufarbeitungen für prognostische Information
Die Diagnose wird dann in der Regel klinisch, das heißt ohne Biopsie, gestellt.
Sofern die Diagnose gestellt wurde, sollte überprüft werden, ob die Erkrankung nur das Auge betrifft oder bereits Organabsiedelungen (=Metastasen) nachzuweisen sind. Da die Metastasierung in den meisten Fällen die Leber betrifft, werden Laboruntersuchungen (wie z.B. Bestimmung der Leberwerte) und bildgebende Untersuchungen der Bauchorgane (z.B. Sonografie der Leber) empfohlen.
Wann ist eine Biopsie notwendig oder sinnvoll?
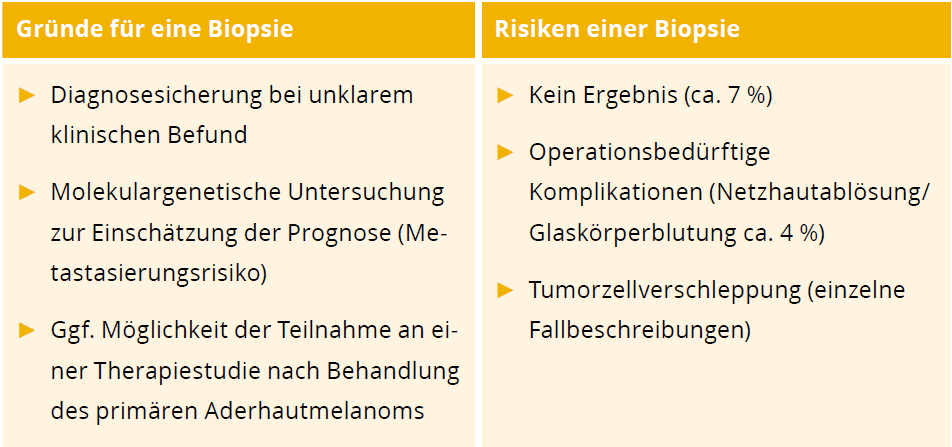
Die meisten Fälle lassen sich anhand von klinischen Kriterien gut in eine gut- oder bösartige Kategorie einordnen. In wenigen unklaren Fällen kann eine Biopsie, d. h. eine Gewebeprobe des Tumors zur Diagnosefindung sinnvoll sein. Außerdem kann eine Gewebeprobe erwogen werden, um zusätzlich zur histopathologischen Diagnosesicherung die Prognose, d. h. das Risiko für eine Metastasierung abzuschätzen. Dafür wird das Gewebe molekulargenetisch untersucht. Siehe auch Abschnitt: Genetik des Aderhautmelanoms, S. 15 im Patientenratgeber_Uvea-Melanom_2025_final.pdf
Diese Methode birgt jedoch auch Risiken. Insbesondere bei kleineren Befunden liefert die Probenentnahme nicht immer ein eindeutiges Ergebnis (ca. 7 %). Außerdem treten bei etwa 4% der Patienten Netzhautablösungen oder Einblutungen auf, die das Sehen beeinträchtigen können. In einzelnen, sehr seltenen Fällen tritt im Anschluss an eine Biopsie eine Verschleppung von Tumorzellen im Auge auf.
Patienten mit der Diagnose eines Aderhautmelanoms beschreiben häufig unspezifische Symptome und Sehstörungen.
Die Diagnose des Aderhautmelanoms wird in der Regel klinisch gestellt.
- REFERENZEN
- [6] Bechrakis et al.: Das uveale Melanom – standardisiertes Vorgehen in Diagnostik, Therapie und Nachsorge. Klin Monbl Augenheilkd. 2021
INTERESSENSKONFLIKTE
Der Autor/die Autorin hat keine Interessenskonflikte angegeben.
Behandlung des Aderhautmelanoms
Zuletzt aktualisiert: 05.05.2025 | Autor(in): Max Schlaak, Markus Heppt
Die Behandlung eines Aderhautmelanoms zielt darauf ab, den Tumor zu zerstören und das bei Diagnosestellung bereits vorhandene Risiko einer Metastasierung nicht durch weiteres Tumorwachstum zu erhöhen und, wenn möglich, das Auge und das Sehvermögen zu erhalten.
Strahlentherapie
Die Bestrahlung ist die Therapie der Wahl für die meisten Patienten/Patientinnen mit primärem Aderhautmelanom. Dabei ist das Ziel, den Tumor am Auge zu zerstören und dabei das umliegende Gewebe bestmöglich zu schonen. Es gibt verschiedene Ansätze:
Brachytherapie (Plaque-Strahlentherapie): Eine kleine Strahlenquelle wird direkt auf das Auge aufgenäht, um den Tumor gezielt zu bestrahlen. [9]
- Vorteile: Hohe Erfolgsquote bei kleinen bis mittelgroßen Tumoren
- Nebenwirkungen: Strahlenbedingte Nebenwirkungen am Auge, die zu einer Sehminderung führen können
Protonenstrahltherapie: Hochenergetische Protonenstrahlen zerstören gezielt den Tumor, während das umliegende Gewebe geschont wird.
- Vorteile: Präzise Methode, mit der man Tumore jeglicher Größe und Lage behandeln kann
- Nebenwirkungen: Strahlenbedingte Nebenwirkungen am Auge, die zu einer Sehminderung führen können
Stereotaktische Strahlentherapie (CyberKnife, Gamma Knife, LINAC): CyberKnife, Gamma Knife und LINAC nutzen fokussierte Photonenstrahlen, um den Tumor zu bestrahlen.
- Vorteile: Neuere Methode, mit der man Tumore jeglicher Größe und Lage behandeln kann
- Nebenwirkungen: Strahlenbedingte Nebenwirkungen am Auge, die zu einer Sehminderung führen können
Bei einer Fractionated Stereotactic Radiation Therapy (Abkürzung: fSRT) werden mehrere kleinere Strahlendosen verabreicht, was die Nebenwirkungen ggfs. reduzieren kann. Aktuell ist die Datenlage zur Behandlung am Auge bei diesem Tumor recht gering. Man geht von einer Gleichwertigkeit bzgl. der lokalen Tumorkontrolle bei allen Verfahren aus. Unklar ist, ob ein Verfahren für den Erhalt der Sehleistung nach Behandlung besser geeignet ist.[10] In Zukunft sind weitere vergleichende Studien gewünscht, um hier die optimale Behandlung für Patienten und Patientinnen zu definieren.
Ergänzende Lasertherapie (TTT): Nach der Strahlentherapie kann eine transpupilläre Thermotherapie (TTT) mittels Infrarot-Laser eingesetzt werden, um Tumorreste mit Restaktivität zu zerstören.
Operation
Lokale Tumorresektion (Endoresektion): Diese Methode wird bei großen Tumoren angewendet, um das Risiko schwerer Entzündungen durch Abbauprodukte nach der Bestrahlung zu minimieren und somit die Chance auf einen Augenerhalt nach einer Bestrahlung zu erhalten. Ziel des Eingriffs ist hier der Versuch des Augenerhalts bei guter Tumorkontrolle.[6]
- Vorteile: Entfernung großer Tumoren, Vermeidung schwerer Entzündungen
- Nebenwirkungen: Hohe chirurgische Komplexität, häufig Revisionsoperationen notwendig
Enukleation (Entfernung des Auges): Diese Methode wird eingesetzt, wenn der Tumor sehr groß ist oder das Auge bereits stark geschädigt wurde. Sie bietet jedoch keinen Überlebensvorteil gegenüber augenerhaltenden Behandlungsmethoden.
- Vorteile: Sicherste Methode zur Tumorentfernung
- Nebenwirkungen: Verlust des Auges und emotionale Belastung
Medikamentöse Therapie
Derzeit gibt es keine zugelassenen systemischen Therapien für den Primärtumor. Genetische Untersuchungen können jedoch Hinweise auf das Metastasierungsrisiko geben und zukünftige Therapieansätze beeinflussen. In klinischen Studien werden neoadjuvante und adjuvante Therapieansätze geprüft, d.h. eine medikamentöse Therapie vor der Operation (neo-adjuvant) oder im Anschluss an die Operation (adjuvant), mit dem Ziel, den Tumor augenerhaltend behandeln zu können und das Metastasierungsrisiko zu verringern.
Fazit
Die Behandlung des Aderhautmelanoms erfordert als seltene Tumorerkrankung eine komplexe und interdisziplinäre medizinische Behandlung in spezialisierten Zentren. Die guten und langjährig etablierten strahlentherapeutischen Therapien können durch moderne Maßnahmen wie Lasertherapie, durch chirurgische Eingriffe oder medikamentöse Therapien ergänzt werden. Das Ziel ist dabei immer, den Augenerhalt zu gewährleisten, das Sehvermögen zu erhalten und eine bestmögliche Tumorkontrolle zu ermöglichen. Dies gelingt in den überwiegenden Fällen.
Die Behandlung des Aderhautmelanoms richtet sich nach der Lokalisation und Größe des Tumors.
Verschiedene Therapieoptionen zur intraokulären Tumorbehandlung stehen zur Verfügung.
- REFERENZEN
- [6] Bechrakis et al.: Das uveale Melanom – standardisiertes Vorgehen in Diagnostik, Therapie und Nachsorge. Klin Monbl Augenheilkd. 2021
- [9] Lalos F. et al. (2025). Tumor- and treatment-related complications after Ruthenium-106 brachytherapy in small to medium uveal melanomas. Klinische Monatsblätter für Augenheilkunde.
- [10] Erikson et al. Evaluation of ocular and systemic endpoints after radiation of posterior uveal melanoma - A systematic review and meta-analysis Heliyon. 2024 Aug 22;10(18)
INTERESSENSKONFLIKTE
Der Autor/die Autorin hat keine Interessenskonflikte angegeben.
Einschätzung der Prognose beim Aderhautmelanom
Zuletzt aktualisiert: 14.04.2026 | Autor(in): Max Schlaak, Markus Heppt
Genetik des Aderhautmelanoms
Das Erbgut einer Zelle, die sogenannten Gene, sind wie eine Art „Anleitung“ für die Zelle, wie sie z. B. zu wachsen oder sich zu teilen hat. Manchmal können in diesen „Anleitungen“ Fehler entstehen, entweder durch Zufall oder durch äußere Einwirkungen, wie z. B. UV-Licht, was dazu führen kann, dass die Zelle nicht mehr richtig funktioniert. Diese Fehler werden Mutationen genannt. Sie können entweder vererbt werden („Keimbahnmutationen“) oder im Laufe des Lebens zufällig auftreten, d. h. sie werden erworben („somatisch“).
Wenn eine fehlerhafte Zelle beginnt, sich unkontrolliert zu vermehren, entsteht ein Tumor. Eine Tumormutation ist also ein Fehler im Gen, der dazu führt, dass eine Zelle sich zu schnell und unkontrolliert teilt. Im Rahmen der Tumorentstehung kann es auch zu sogenannten chromosomalen Veränderungen kommen, bei denen mehrere Gene gleichzeitig beeinflusst werden. Diese Veränderungen können dazu führen, dass bestimmte Gene überaktiv oder unteraktiv sind, was die Prognose der Erkrankung beeinflussen kann.
Beim Aderhautmelanom gibt es spezifische genetische Veränderungen, die wichtig für die Prognose und das Risiko von Metastasen sind.[11,12] Für eine genetische Analyse wird Tumormaterial gebraucht, das entweder mittels Biopsie aus dem Auge (hier entsprechende Verlinkung auf dem Infoportal oder Weglassen) oder bei der operativen Entfernung des Tumores gewonnen wird.


Risikogruppen
Die Einteilung der Patienten in Risikogruppen basiert sowohl auf der TNM-Klassifikation als auch auf den genetischen Veränderungen des Tumors:

Die Bestimmung der Risikogruppe kann ggf. auch sinnvoll sein, um zu prüfen, ob Sie für eine adjuvante Therapie, z. B. im Rahmen einer klinischen Studie in Frage kommen, um das Rückfallrisiko für PatientInnen mit hohem Risiko zu verringern. Doch was bedeutet „hohes Risiko“ überhaupt für Sie als Betroffene oder Betroffener? Wie sicher sind diese Aussagen – und welche nächsten Schritte ergeben sich daraus?
Ich bin Hochrisikopatient – was bedeutet das für mich?
Diese Frage beschäftigt viele Betroffene – und es ist völlig verständlich, dass Sie sich mehr Orientierung wünschen. Fachleute sprechen dann von sogenannten „HochrisikopatientInnen“, wenn bestimmte Merkmale vorliegen, die statistisch mit einem höheren Risiko für eine Metastasierung – also das Streuen des Tumors in andere Organe – verbunden sind.
Was sind Risikofaktoren?
Die wichtigsten Risikofaktoren lassen sich in zwei Gruppen einteilen:
- Klinische Merkmale
Dazu gehören unter anderem:- die Größe und Ausbreitung des Tumors,
- seine Lokalisation im Auge,
- bestimmte Gewebeeigenschaften (z. B. ein sogenannter epitheloidzellartiger Zell typ oder das Vorhandensein spezieller Gefäßstrukturen).
Ein Tumor im sogenannten Stadium III (laut TNM-Klassifikation) wird klinisch als Hochrisikotumor eingestuft.
- Genetische Merkmale
Bei einem Aderhautmelanom kann das Erbgut des Tumors untersucht werden. Dabei zeigt sich bei manchen PatientInnen eine sogenannte Monosomie 3 – das bedeutet, dass das Chromosom 3 nur einmal (statt wie üblich zweimal) vorhanden ist. Diese Veränderung wird mit einem erhöhten Risiko für Metastasen in Verbindung gebracht.
Wichtig: Eine Monosomie 3 bedeutet nicht, dass Metastasen sicher auftreten – und ein „normaler“ Chromosomensatz garantiert keine Metastasenfreiheit. Es handelt sich immer um Wahrscheinlichkeiten, nicht um Gewissheiten.
Wie wird das Risiko bestimmt?
Um festzustellen, ob eine genetische Hochrisikosituation vorliegt, muss Tumorgewebe untersucht werden. Das passiert entweder im Rahmen einer Entfernung des Auges oder durch eine gezielte Gewebeentnahme (Biopsie). An spezialisierten Zentren stehen dafür verschiedene Verfahren zur Verfügung. Ob und wann eine solche Untersuchung sinnvoll ist, wird mit Ihnen gemeinsam in einem augenonkologischen Zentrum besprochen.
Warum ist das Wissen um das Risiko wichtig?
Wenn bekannt ist, dass ein erhöhtes Risiko vorliegt, können Sie gemeinsam mit Ihren behandelnden Ärzten und Ärztinnen bestimmte Schritte in die Wege leiten:
Vorteile
- Intensivere Nachsorge: HochrisikopatientIinnen können auf Wunsch engmaschiger auf Metastasenneubildungen untersucht werden – z. B. alle drei Monate –, um mögliche Metastasen frühzeitig zu erkennen.
- Teilnahme an Studien: In spezialisierten Zentren werde klinische Studien angeboten, die neue Behandlungsmöglichkeiten oder unterstützende Maßnahmen untersuchen – speziell für PatientInnen mit hohem Risiko.
- Informierte Entscheidungen: Je besser Sie über Ihre individuelle Situation Bescheid wissen, desto aktiver können Sie in Ihre Behandlung und Nachsorge einbezogen werden.
Nachteil
- Emotionale Belastung: Die Bezeichnung "Hochrisiko" ist noch keine Diagnose – es ist eine Einschätzung, die bei der Wahl der besten Behandlung und Nachsorge hilft. Ihr Ärzteteam wird mit Ihnen gemeinsam besprechen, was das in Ihrem Fall bedeutet – und welche Schritte sinnvoll sind.
INTERESSENSKONFLIKTE
Der Autor/die Autorin hat keine Interessenskonflikte angegeben.
Nachsorge beim Aderhautmelanom
Zuletzt aktualisiert: 14.04.2026 | Autor(in): Max Schlaak, Markus Heppt
Bedeutung der Risikogruppen für die Nachsorge
Die Nachsorge hat das Ziel, Lokalrezidive im Auge zu erkennen und möglichst frühzeitig eine Absiedelung in Organe festzustellen. Da das Aderhautmelanom sehr häufig (> 90 %) in die Leber metastasiert und die Leber meist das erste betroffene Organ ist, ist die Untersuchung dieses Organs von besonderer Bedeutung.
Alle Patienten sollten unabhängig vom Risikoprofil nachgesorgt werden. Die Häufigkeit und auch die Art der Nachsorge kann dabei je nach Risikoprofil anders aussehen. Während bei niedrigem Risiko ein halbjährlicher Ultraschall der Leber ausreichend sein kann, wird Patienten mit hohem Metastasierungsrisiko eine engmaschigere Nachsorge, z.B. alle 3 Monate angeboten.
Optional sind die Bestimmung der Leberwerte (LDH, GOT, GPT, Gamma-GT, Bilirubin, alkalische Phosphatase). Findet sich ein auffälliger Befund ist eine Bildgebung der Leber mittels MRT erforderlich. Unklar ist derzeit, wie lange eine Nachsorge durchgeführt werden sollte. Da Krankheitsrückfälle am häufigsten in den ersten fünf Jahren nach der Erstdiagnose auftreten, sollte die engmaschige Nachsorge mindestens in diesem Zeitraum erfolgen. Danach ist dieses individuell festzulegen.
Beispiel für ein Nachsorgeschema
Augenärztliche Nachsorge

Diese Nachsorgeintervalle können von dem erfahrene/n Augenarzt/-ärztin abhängig vom klinischen Befund angepasst bzw. verkürzt werden. Für kleine und mittlere Tumoren ist eine Nachsorge für eine Streuungssuche (Metastasenfindung) wie folgt empfohlen:
Für große Tumoren (ab St. III) ist eine Nachsorge wie folgt empfohlen:
Diese Nachsorgeintervalle können von dem tumorerfahrenen versorgenden Arzt/Ärztin abhängig vom klinischen Befund angepasst bzw. verkürzt werden. Generell gilt, dass nur sinnhafte Nachsorgekontrolltermine angesetzt werden sollen, da ein unnötiger Kontrolltermin durchaus negative Effekte auf die Lebensqualität des/der Patienten/in hat. Der/Die behandelnde Arzt/Ärztin sollte daher die Kontrollintervalle mit dem/der Patienten/in abstimmen.
Die Nachsorge für Patienten und Patientinnen mit Aderhautmelanom ist noch nicht einheitlich geregelt.
Es sollte versucht werden, die Nachsorge am individuellen Risikoprofil des Aderhautmelanoms auszurichten. Leider ist das individuelle Risikoprofil nicht immer bekannt. Patienten bzw. Patientinnen mit einem hohen Risiko, (z.B. genetische Veränderungen, Tumorgröße) Metastasen zu bilden, sollten nach Möglichkeit häufiger kontrolliert werden. Nach Diagnose und Therapie des Primärtumors sollten alle Patienten eine regelmäßige Nachsorge erhalten, auch wenn die Dauer und Häufigkeit der Untersuchungen nicht standardisiert ist.
Als Kontrolluntersuchungen werden empfohlen:
- Abfrage von Allgemeinsymptomen
- Körperliche Untersuchung und Ganzkörperinspektion
- Bestimmung der Leberwerte alle 3-6 Monate
- Sonografische (Ultraschall-basierte) Kontrollen der Leber alle 3-6 Monate
- Augenärztliche Kontrolluntersuchungen
Die Nachsorge nach einer Behandlung des Aderhautmelanoms sollte sich an dem Risikoprofil orientieren.
Insbesondere Kontrollen der Leber sind wichtig.
- REFERENZEN
- [6] Bechrakis et al.: Das uveale Melanom – standardisiertes Vorgehen in Diagnostik, Therapie und Nachsorge. Klin Monbl Augenheilkd. 2021
INTERESSENSKONFLIKTE
Der Autor/die Autorin hat keine Interessenskonflikte angegeben.
Das metastasierte Aderhautmelanom
Zuletzt aktualisiert: 14.04.2026 | Autor(in): Max Schlaak, Markus Heppt
Im Fall einer Metastasierung empfiehlt sich eine Anbindung an ein Zentrum, an dem eine größere Anzahl von Patienten bzw. Patientinnen mit metastasierten Aderhautmelanom behandelt wird. Im Regelfall werden die Patientenfälle in einem interdisziplinären Gremium besprochen und gemeinsam Therapieempfehlungen vereinbart.
Sofern nur einzelne Metastasen vorliegen, kann ein operatives Vorgehen diskutiert werden. Wenn die Leber als häufigster Metastasierungsort alleine betroffen ist, können lokale Behandlungen an der Leber in Frage kommen. Eine lokale Behandlung bedeutet, dass die Therapie vor allem am betroffenen Organ wirksam werden soll und gesunde Organe möglichst geschont werden. Hier stehen verschiedene Behandlungen je nach Zentrum zur Verfügung, wie z.B. die transarterielle Chemoembolisation (TACE), die selektive interne Radiotherapie (SIRT), Chemosaturation der Leber und verschiedene andere Behandlungsformen. Eine eindeutige Präferenz für eine der Behandlungen gibt es aktuell noch nicht.
Wie bereits beschrieben wirken die medikamentösen Therapien nicht so effektiv wie bei Patienten bzw. Patientinnen mit Melanomen der Haut. Daher sollte ein individuelles Therapiekonzept erstellt werden und eine Teilnahme an einer klinischen Studie besprochen werden.
Eine medikamentöse Therapiemöglichkeit des metastasierten Aderhautmelanoms stellt Tebentafusp dar. In einer Phase III Studie für Patientinnen und Patienten mit metastasiertem Aderhautmelanom und einem bestimmten Zelloberflächenmarker (sogenannter positiver HLA-A 02:01 Status) wurde Tebentafusp gegenüber Dacarbazin, Ipilimumab oder Pembrolizumab untersucht. Der Nachweis des genannten Markers ist notwendig für die Funktion des Medikaments und liegt bei ca. 30-40% der Bevölkerung in Mitteleuropa vor. Nach einem Jahr lebten 73% der Patientinnen und Patienten in der Tebentafusp-Gruppe und 59% in der Kontrollgruppe. Nebenwirkungen sind gerade am Anfang der Behandlung häufig, aber in der Regel beherrschbar (7). Basierend auf diesen Studienergebnissen wurde Tebentafusp (Handelsname Kimmtrak) im April 2022 in der EU zur Behandlung des metastasierten Aderhautmelanoms zugelassen. Es handelt sich dabei um eine Infusionstherapie, die einmal wöchentlich verabreicht wird. Kürzlich wurden auch Ergebnisse der Studie nach einer dreijährigen Nachbeobachtungszeit veröffentlicht. Nach dieser Zeit war das mittlere Gesamtüberleben im Behandlungsarm mit Tebentafusp 21,6 Monate gegenüber 16,9 Monaten in den Vergleichsgruppen. Nach 3 Jahren waren im Durchschnitt noch 27% am Leben, in den Vergleichsarmen nur 18%. Tebentafusp stellt damit eine deutliche Verbesserung in der Behandlung des metastasierten Aderhautmelanoms mit einer gut belegten Verbesserung des Gesamtüberlebens dar (8).
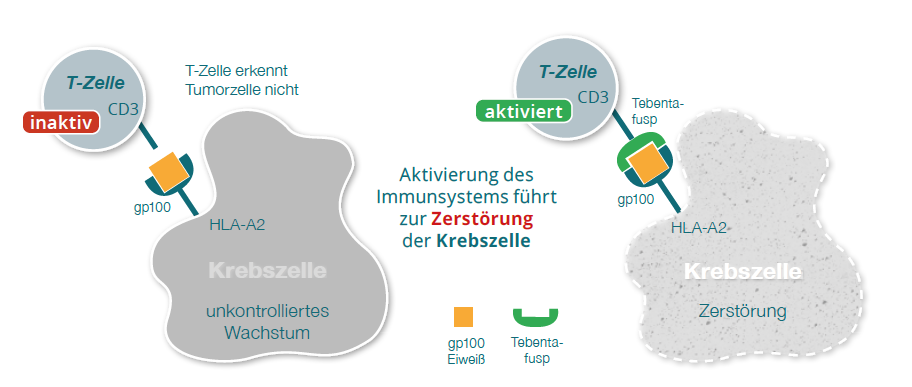
Therapie mit Tebentafusp
Im metastasierten Stadium stehen verschiedene Therapieoptionen zur Verfügung. Häufig werden bei einem alleinigen Befall der Leber lokale Therapieverfahren eingesetzt.
Bei Nachweis des HLA-Typs 02:01 im Blut ist die zugelassene Standardtherapie Tebentafusp.
- REFERENZEN
- [1] Servier Medical Arts
- [2] Mallone et al.: Descriptive epidemiology of malignant mucosal and uveal melanomas and adnexal skin carcinomas in Europe. Eur J Cancer. 2012
- [3] Coupland et al.: Molecular pathology of uveal melanoma. Eye (Lond). 2013
- [4] Van Raamsdonk et al.: Frequent somatic mutations of GNAQ in uveal melanoma and blue naevi. Nature. 2009
- [5] Van Raamsdonk et al.: Mutations in GNA11 in uveal melanoma. N Engl J Med. 2010
- [6] Bechrakis et al.: Das uveale Melanom – standardisiertes Vorgehen in Diagnostik, Therapie und Nachsorge. Klin Monbl Augenheilkd. 2021
- [7] Nathan et al.: Overall Survival Benefit with Tebentafusp in Metastatic Uveal Melanoma. N Engl J Med. 2021
- [8] Hassel et al.: Three-Year Overall Survival with Tebentafusp in Metastatic Uveal Melanoma. N Engl J Med. 2023
- [9] Lalos F. et al. (2025). Tumor- and treatment-related complications after Ruthenium-106 brachytherapy in small to medium uveal melanomas. Klinische Monatsblätter für Augenheilkunde.
- [10] Erikson et al. Evaluation of ocular and systemic endpoints after radiation of posterior uveal melanoma - A systematic review and meta-analysis Heliyon. 2024 Aug 22;10(18)
INTERESSENSKONFLIKTE
Der Autor/die Autorin hat keine Interessenskonflikte angegeben.
Wo finde ich Unterstützung?
Zuletzt aktualisiert: 05.05.2025 | Autor(in): Max Schlaak
- Austauschgruppe „Diagnose Aderhautmelanom - wir lassen dich nicht allein“
- https://www.krebsgesellschaft.de
- https://www.krebsinformationsdienst.de
- https://www.esmo.org/for-patients (englisch)
- https://thinkuvealmelanoma.com/ (englisch, Industrie)
- https://www.facebook.com/groups/437126616930687/?ref=share/
- https://www.facebook.com/groups/MPNEOcularRare/?ref=share/
- Broschüre „„Aderhautmelanom – Ein Ratgeber für Patientinnen und Patienten“
INTERESSENSKONFLIKTE
Der Autor/die Autorin hat keine Interessenskonflikte angegeben.
Link copied to clipboard!